研究概要
3)配座変換型不斉有機触媒の開発と利用
有機合成化学において「触媒」というと有機金属錯体や酵素が思い浮かびますが、小さな有機分子もまた、酸、塩基触媒を始めさまざまな触媒として作用することが古くから知られていました。 有機触媒は、設計や合成の自由度が大きいため構造的多様性を有し、基質にフィットしたテーラーメイド触媒としての発展も期待されます。 さらに金属を使用しないため触媒の処理が容易であり、グリーンケミストリーにも貢献すると考えられます。 不斉有機触媒の研究は注目されてからまだ日が浅いにもかかわらず、すでに様々なタイプの化合物が有効な触媒として作用する事が明らかにされ、 高い選択性や回転数を示すものが続々報告されてきています。
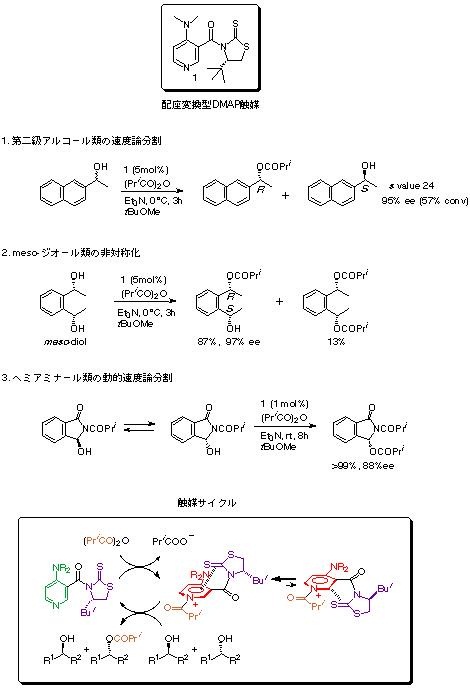
私たちも、新しいタイプの有機触媒の研究を行っていますが、分子内カチオン-π相互作用を触媒の立体配座制御に利用することで、 立体選択性ならびに触媒活性を制御できるものと考えています。 分子内相互作用を利用することで、活性中心から遠隔位の不斉炭素により触媒のキラリティーを制御可能であり、基質との反応後は触媒の運動の自由度を取り戻すことで、触媒活性の低下を回避できると考えられます。 我々は、このような考え方に基づき種々の触媒設計を検討しています。 以下に配座変換型DMAP触媒1を用いる様々なアルコール類の不斉アシル化について紹介します。 0.05-5 mol%の触媒存在下、 イソ酪酸無水物を用いて種々の第二級アルコールの不斉アシル化を検討した結果、 速度論分割、動的速度論分割、非対称化反応において、いずれも高い選択性で不斉アシル化を達成できました。
本反応の機構は下図のように考えています。 触媒がN-アシル化されることでカチオン-π錯体を形成し、不斉炭素が活性部位から離れているにもかかわらずキラルな環境が形成されます。 アルコールは遮蔽されていない側からアシル基を攻撃し、このときアルコールの立体化学が識別されると考えられます。 脱アシル化に伴い、触媒は自由度を取り戻し次のサイクルが始まります。このように触媒サイクルの過程で触媒の配座変換が起るため、触媒活性の低下を回避できるものと考えられます。 今後、様々なタイプの配座変換型触媒を開発していきたいと考えています。
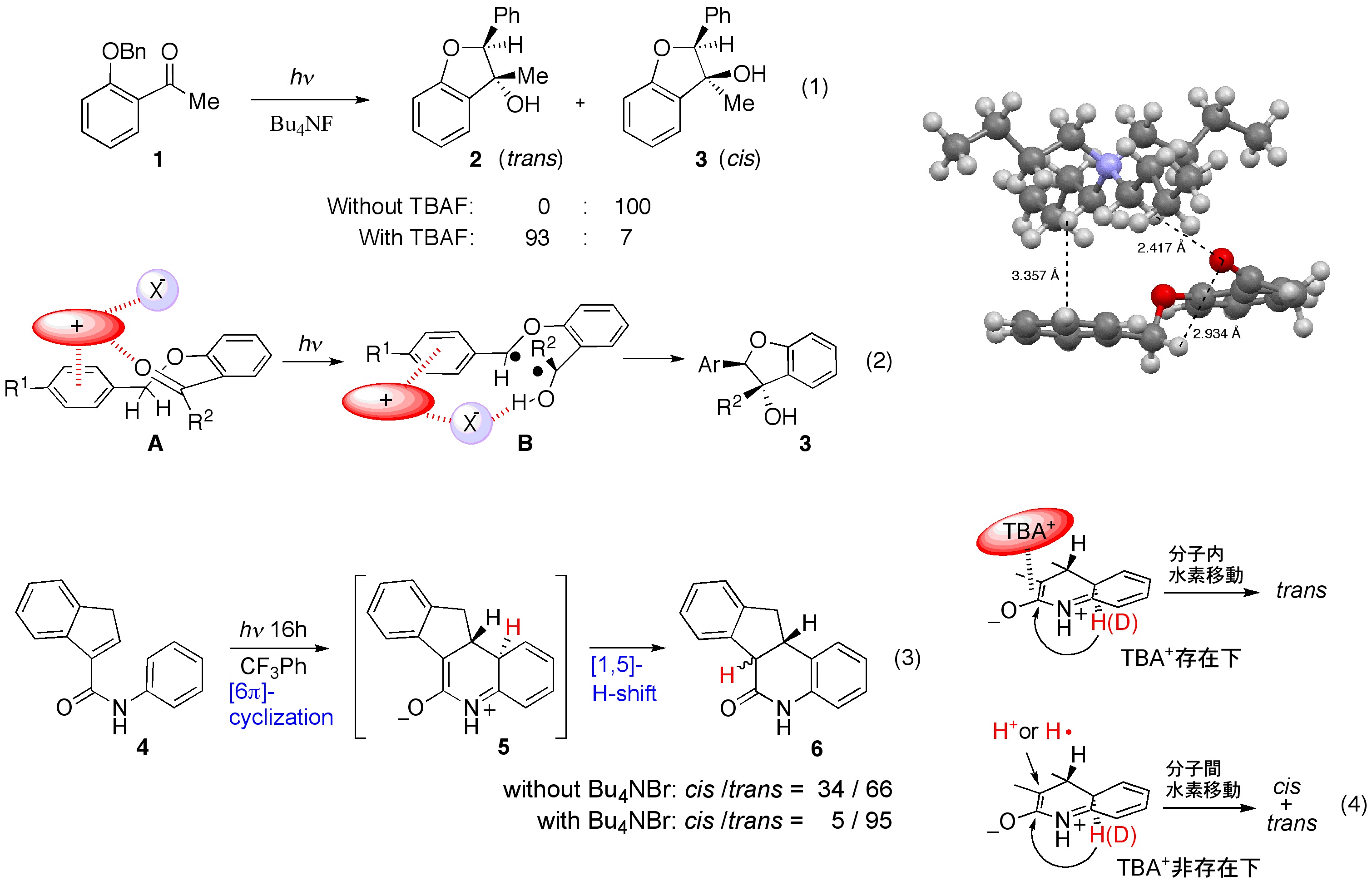
最近、当研究室ではテトラアルキルアンモニウムが様々な光反応の立体選択性を制御することを明らかにしています。テトラアルキルアンモニウムを加えることで、基質のコンホメーションが変化し、Norrish-Yang反応が特定のコンホメーションから進行することで立体選択性が発現することを明らかにしました。また、アクリル酸アニリド類の[6π]光環化反応では、中間体にアンモニウムエノラートが生成することで、分子間水素移動が阻害され、立体選択性が生まれることも明らかにしています。 今後テトラアルキルアンモニウム塩を有機触媒として利用する展開を行っていきたいと考えています。
関連論文
《NEXT》… 4)分子配列制御と固相反応
《PREV》… 2)立体選択的[2+2]光付加環化反応
TOPへ戻る
3)配座変換型不斉有機触媒の開発と利用
有機合成化学において「触媒」というと有機金属錯体や酵素が思い浮かびますが、小さな有機分子もまた、酸、塩基触媒を始めさまざまな触媒として作用することが古くから知られていました。 有機触媒は、設計や合成の自由度が大きいため構造的多様性を有し、基質にフィットしたテーラーメイド触媒としての発展も期待されます。 さらに金属を使用しないため触媒の処理が容易であり、グリーンケミストリーにも貢献すると考えられます。 不斉有機触媒の研究は注目されてからまだ日が浅いにもかかわらず、すでに様々なタイプの化合物が有効な触媒として作用する事が明らかにされ、 高い選択性や回転数を示すものが続々報告されてきています。
私たちも、新しいタイプの有機触媒の研究を行っていますが、分子内カチオン-π相互作用を触媒の立体配座制御に利用することで、 立体選択性ならびに触媒活性を制御できるものと考えています。 分子内相互作用を利用することで、活性中心から遠隔位の不斉炭素により触媒のキラリティーを制御可能であり、基質との反応後は触媒の運動の自由度を取り戻すことで、触媒活性の低下を回避できると考えられます。 我々は、このような考え方に基づき種々の触媒設計を検討しています。 以下に配座変換型DMAP触媒1を用いる様々なアルコール類の不斉アシル化について紹介します。 0.05-5 mol%の触媒存在下、 イソ酪酸無水物を用いて種々の第二級アルコールの不斉アシル化を検討した結果、 速度論分割、動的速度論分割、非対称化反応において、いずれも高い選択性で不斉アシル化を達成できました。
本反応の機構は下図のように考えています。 触媒がN-アシル化されることでカチオン-π錯体を形成し、不斉炭素が活性部位から離れているにもかかわらずキラルな環境が形成されます。 アルコールは遮蔽されていない側からアシル基を攻撃し、このときアルコールの立体化学が識別されると考えられます。 脱アシル化に伴い、触媒は自由度を取り戻し次のサイクルが始まります。このように触媒サイクルの過程で触媒の配座変換が起るため、触媒活性の低下を回避できるものと考えられます。 今後、様々なタイプの配座変換型触媒を開発していきたいと考えています。

最近、当研究室ではテトラアルキルアンモニウムが様々な光反応の立体選択性を制御することを明らかにしています。テトラアルキルアンモニウムを加えることで、基質のコンホメーションが変化し、Norrish-Yang反応が特定のコンホメーションから進行することで立体選択性が発現することを明らかにしました。また、アクリル酸アニリド類の[6π]光環化反応では、中間体にアンモニウムエノラートが生成することで、分子間水素移動が阻害され、立体選択性が生まれることも明らかにしています。 今後テトラアルキルアンモニウム塩を有機触媒として利用する展開を行っていきたいと考えています。

関連論文
- S. Yamada, Y. Oshima, Y. Fujita, S. Tsuzuki, Tetrahedron Lett. 2019, 60, 1543-1546.
- S. Yamada, M. Okuda, N. Yamamoto,“Tetrabutylammonium-assisted diastereoselective [6π]-photocyclization of acrylanilides”, Tetrahedron Lett., 2015, 56, 2098-2101
- S. Yamada, A. Iwaoka, Y. Fujita, S. Tsuzuki,“Tetraalkylammonium-Templated Stereoselective Norrish-Yang Cyclization”, Org. Lett., 2013, 15, 5994-5997
- Y. Mori and S. Yamada,“Contribution of Cation-π Interactions in Iminium Catalysis”, Molecules, 2012, 17, 2161-2168
- S. Yamada and J. S. Fossey,“Nitrogen cation-π interactions in asymmetric organocatalytic synthesis”, Org. Biomol. Chem., 2011, 9, 7257-7580
- S. Yamada, K. Yamashita,“Dynamic Kinetic Resolution of Hemiaminals Using a Novel DMAP Catalyst”, Tetrahedron Lett., 49, 32-35 (2008).
- S. Yamada, T. Misono, Y. Iwai, A. Masumizu, Y. Akiyama,“A New Class of Pyridine Catalyst Having a Conformation Switch System: Asymmetric Acylation of Various sec-Alcohols”, J. Org. Chem., 71, 6872-6880 (2006).
- S. Yamada, T. Misono, Y. Iwai "Kinetic resolution of sec-alcohols by a new class of pyridine catalysts having a conformation switch system" Tetrahedron Lett., 46, 2239-2242 (2005).
- S. Yamada, T. Misono, S. Tsuzuki "Cation-π interaction of a Thiocarbonyl Group and a Carbonyl Group with a Pyridinium Nucleus" J. Am. Chem. Soc., 126, 9862-9872 (2004).
《NEXT》… 4)分子配列制御と固相反応
《PREV》… 2)立体選択的[2+2]光付加環化反応
TOPへ戻る